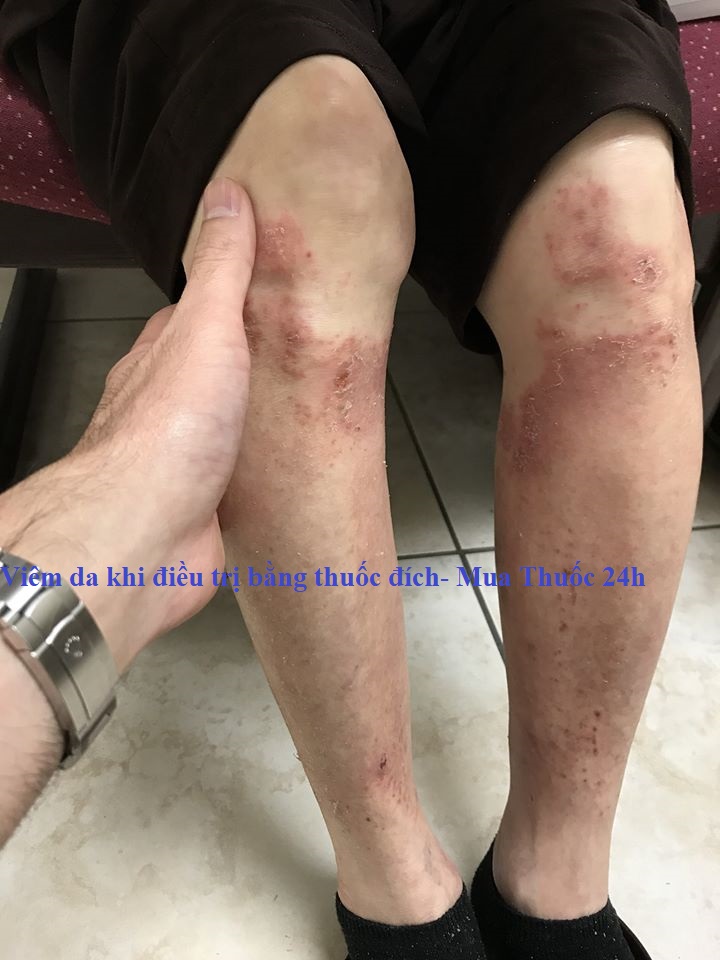
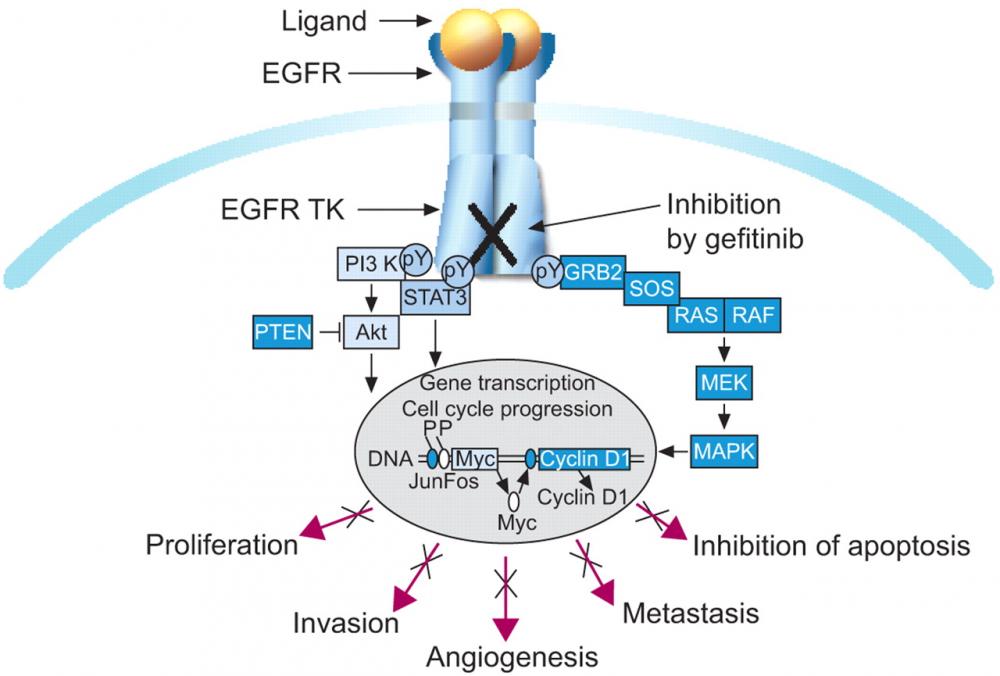
Phân loại các thuốc đích điều trị ung thư nhóm ức chế EGFR-TKI
Thuốc đích nhóm ức chế EGFR-TKI hiện là một trong các phương pháp điều trị ung thư hiệu quả và ít tác dụng phụ. Kể từ khi phê duyệt EGFR-TKI đầu tiên vào năm 2003, một số lượng lớn các chất ức chế EGFR đã được báo cáo. Phân loại các chất ức chế này có thể giúp các nhà nghiên cứu hiểu được mối quan hệ cấu trúc-hoạt động của chúng. Ở đây, chúng tôi giới thiệu các loại phân loại khác nhau của EGFR-TKIs, đã nhận được sự chấp thuận toàn cầu cho sử dụng lâm sàng. Sau đây, các loại thuốc nhắm mục tiêu EGFR được phân loại dựa trên hóa học, sử dụng lâm sàng, kinase đích và loại ức chế / tương tác với EGFR.
Chất ức chế kinase EGFR được phân loại theo mấy phương pháp sau: Phân loại hóa học, phân loại dược lý, phân loại dựa trên kinase mục tiêu, phân loại dựa trên ức chế / tương tác
Phân loại hóa học
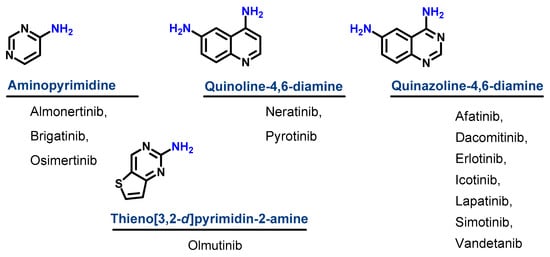
Dựa trên cấu trúc hóa học của chúng, các EGFR-TKI đã được phê duyệt có thể được phân thành ba phân lớp. Phân lớp đầu tiên là các dẫn xuất aminopyrimidine bao gồm almonertinib, brigatinib và osimertinib. Trong nghiên cứu này, olmutinib được coi là một dẫn xuất aminopyrimidine hợp nhất. Nhóm thứ hai có nhân quinoline-4,6-diamine và bao gồm hai dẫn xuất, neratinib và pyrotinib. Nhóm thứ ba là các dẫn xuất dựa trên quinazoline-4,6-diamine bao gồm afatinib, dacomitinib, erlotinib, icotinib, lapatinib, simotinib và vandetanib.
Phân loại dựa trên các loại tương tác với EGFR
Dựa trên loại ức chế hoạt động của EGFR, các EGFR-TKI đã được phê duyệt cũng có thể được phân loại là chất ức chế đảo ngược và không thể đảo ngược, như thể hiện trong Hình 5. Đối với loại đầu tiên, các chất ức chế liên kết cạnh tranh với vị trí liên kết ATP trong EGFR thông qua các tương tác không cộng hóa trị liên quan đến tĩnh điện, liên kết hydro và tương tác kỵ nước.
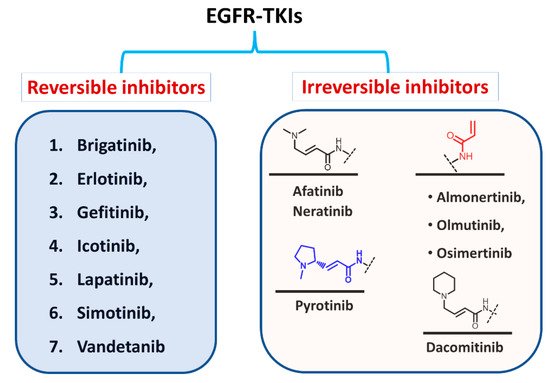
Trong loại thứ hai, các chất ức chế EGFR tạo thành liên kết cộng hóa trị với dư lượng cysteine trong EGFR. Cấu trúc của các chất ức chế này được đặc trưng bởi sự hiện diện của chuỗi bên ưa điện hoạt động như một chất chấp nhận Michael, phản ứng hóa học với nhóm thiol cysteine để tạo thành một chất bổ sung cộng hóa trị.
Phân loại dựa trên sử dụng lâm sàng
Các chất ức chế EGFR cũng có thể được phân thành ba nhóm dựa trên các loại ung thư mà chúng đã được phê duyệt. Nhóm đầu tiên bao gồm các loại thuốc đã được phê duyệt để điều trị NSCLC như afatinib, almonertinib, brigatinib, dacomitinib, erlotinib, gefitinib, icotinib, olmutinib và osimertinib. Loại thứ hai bao gồm các loại thuốc được phê duyệt để điều trị ung thư vú như lapatinib và neratinib, và pyrotinib. Mặt khác, nhóm thứ ba bao gồm các loại thuốc được phê duyệt cho các loại ung thư khác như ung thư tuyến giáp (vandetanib), ung thư tuyến tụy (erlotinib) và ung thư rắn (simotinib).
Phân loại dựa trên kinase mục tiêu
Các EGFR-TKI đã được phê duyệt cũng có thể được phân loại theo kinase mục tiêu của chúng thành chất ức chế EGFR chọn lọc nhắm mục tiêu EGFR với tính chọn lọc cao như gefitinib; các chất ức chế EGFR kép như lapatinib có thể nhắm mục tiêu EGFR và ErbB-2; và các chất ức chế đa kinase như brigatinib, pyrotinib và vandetanib. Những loại thuốc này có hoạt tính phổ rộng chống lại nhiều kinase khác với EGFR.
Phân loại theo thế hệ thuốc đích
Thuốc đích thế hệ 1
Trong số các EGFR-TKI đã được phê duyệt, gefitinib, erlotinib, lapatinib và icotinib được phân loại là chất ức chế EGFR thế hệ đầu tiên. Các loại thuốc trong nhóm này liên kết thuận nghịch với miền PTK của EGFR, dẫn đến ức chế sự liên kết của ATP với EGFR và do đó ức chế kích hoạt EGFR và tăng sinh tế bào. Cấu trúc hóa học của bốn loại thuốc bao gồm một hạt nhân quinazoline cơ bản gắn liền với một moiety anilin thay thế, như thể hiện trong.
Thuốc đích thế hệ 2
Mặt khác, afatinib, neratinib và dacomitinib được phân loại là EGFR-TKI thế hệ thứ hai. Ba loại thuốc này chứa một vị trí chấp nhận Michael cho phép chúng liên kết cộng hóa trị với EGFR, dẫn đến sự ức chế không thể đảo ngược hoạt động kinase, mang lại lợi thế so với EGFR-TKI thế hệ đầu tiên. Cấu trúc hóa học của các loại thuốc này bao gồm quinazoline hoặc nhân quinoline mang chuỗi bên crotonamide (vị trí chấp nhận Michael) được thay thế ở carbon đầu cuối bằng nhóm tert-amino.
Thuốc đích thế hệ 3
Các chất ức chế EGFR thế hệ thứ ba bao gồm almonertinib, olmutinib và osimertinib. Cấu trúc hóa học của các loại thuốc này bao gồm một hạt nhân pyrimidine gắn liền với anilino hoặc phenoxy moiety thay thế. Những moieties này mang một nhóm acrylamide, như đã lưu ý ở trên, có thể tạo thành liên kết cộng hóa trị với dư lượng cysteine trong EGFR.
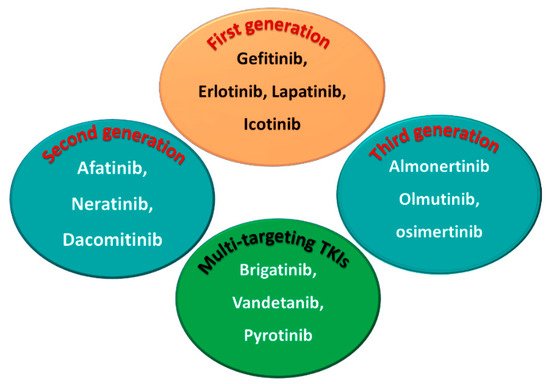
Mặt khác, brigatinib, vandetanib và pyrotinib được phân loại là chất ức chế đa kinase do các hoạt động ức chế của chúng chống lại kinase khác với EGFR.
Sự xuất hiện của đột biến EGFR T790M và C797S đã dẫn đến sự phát triển nhanh chóng của khả năng kháng EGFR-TKI thế hệ thứ nhất, thứ hai và thứ ba. Đột biến C797S cũng làm mất đi các chất ức chế không thể đảo ngược của EGFR về khả năng liên kết cộng hóa trị với kinase. Ngoài ra, sự xuất hiện của đột biến EGFR kép và ba (del19 / L858R + C797S ± T790M) thách thức hiệu quả điều trị của EGFR-TKIs. Những vấn đề này nhấn mạnh nhu cầu liên tục phát triển các EGFR-TKI mới và mạnh mẽ.
Gần đây, một số chất ức chế EGFR allosteric thế hệ thứ tư liên kết với một vị trí trong EGFR khác với miền PTK đã được báo cáo. Tuy nhiên, mặc dù các chất ức chế này không hiệu quả chống lại NSCLC với EGFR đột biến, chúng cho thấy tác dụng chống ung thư hiệp đồng khi kết hợp với chất ức chế EGFR như osimertinib hoặc kháng thể đơn dòng, cetuximab.
Hiện tại, một số EGFR-TKI thế hệ thứ tư đang được đánh giá liên quan đến hiệu quả của chúng đối với các bệnh ung thư mang đột biến EGFR gấp đôi hoặc gấp ba. Một trong những hợp chất này, BBT-176, đang trong các thử nghiệm giai đoạn I / II ở bệnh nhân NSCLC bị ung thư phổi tiến triển, nhưng các chất ức chế này chưa được phê duyệt để sử dụng lâm sàng.
Tác giả bài viết: Dược sĩ Đỗ Thế Nghĩa, Đại Học Dược Hà Nội
Tài liệu tham khảo:
Akher, F.B.; Farrokhzadeh, A.; Soliman, M.E.S. Covalent vs. Non-Covalent Inhibition: Tackling Drug Resistance in EGFR—A Thorough Dynamic Perspective. Chem. Biodivers. 2019, 16, e1800518.
Hossam, M.; Lasheen, D.S.; Abouzid, K.A.M. Covalent EGFR Inhibitors: Binding Mechanisms, Synthetic Approaches, and Clinical Profiles. Arch. Pharm. (Weinh.) 2016, 349, 573–593.
Uribe, M.L.; Marrocco, I.; Yarden, Y. EGFR in Cancer: Signaling Mechanisms, Drugs, and Acquired Resistance. Cancers 2021, 13, 2748.
You, K.S.; Yi, Y.W.; Cho, J.; Park, J.-S.; Seong, Y.-S. Potentiating Therapeutic Effects of Epidermal Growth Factor Receptor Inhibition in Triple-Negative Breast Cancer. Pharmaceuticals 2021, 14, 589.
Dutta, P.R.; Maity, A. Cellular responses to EGFR inhibitors and their relevance to cancer therapy. Cancer Lett. 2007, 254, 165–177.